
2026 年 5 月,国家级领军人才湖南农业大学万发春教授团队的一项研究成果在线发表于国际期刊《Microbiome》(IF=12.7)。该研究以“Microplastics induce liver inflammation in cattle through the rumen microbiota-gut-liver axis”为题,聚乙烯微塑料(PE-MPs)通过“瘤胃微生物 - 肠 - 肝轴”诱发肉牛肝脏炎症的完整机制,填补了反刍动物微塑料毒性研究的关键空白。
研究背景:微塑料(MPs)污染已成为全球农业环境的重大关切。在奶牛养殖过程中,青贮包裹膜、精料编织袋及塑料设备等可释放微塑料进入饲料,其中聚乙烯(PE)是反刍动物饲料中最常见的聚合物类型。然而,PE微塑料对牛的具体毒性机制此前尚未被系统研究。
研究创新点:本研究首次整合宏基因组学、代谢组学和转录组学,系统探究微塑料暴露对牛生长性能、肝脏损伤及肉品安全的影响。
试验设计
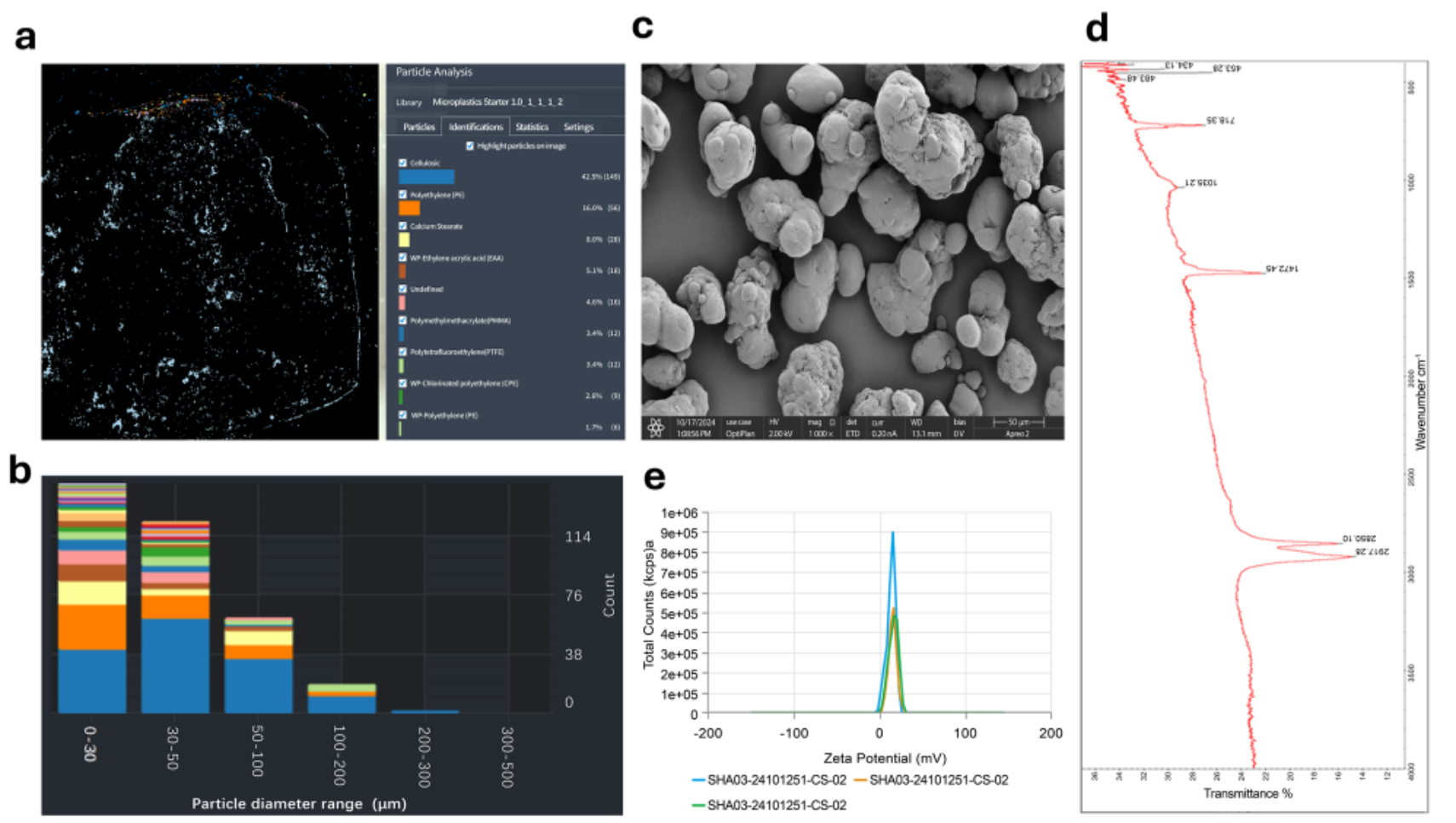
图1 | 青贮饲料中微塑料类型及粒径检测
- (a) 激光直接红外成像(LDIR)化学成像鉴定青贮中的微塑料
- (b) 青贮样品中检测到的微塑料粒径分布(主要<200 μm,<30 μm占比最高)
- (c) 扫描电镜(SEM)观察PE-MPs形貌(球形及不规则形状)
- (d) 傅里叶变换红外光谱(FTIR)确认PE聚合物类型
- (e) PE-MPs的Zeta电位测定(+14.97 mV)
关键发现:青贮中PE占微塑料总数的16%,为主要聚合物类型。据此选择20-200 μm粒径范围的PE颗粒作为试验材料。
生长性能与肝脏损伤
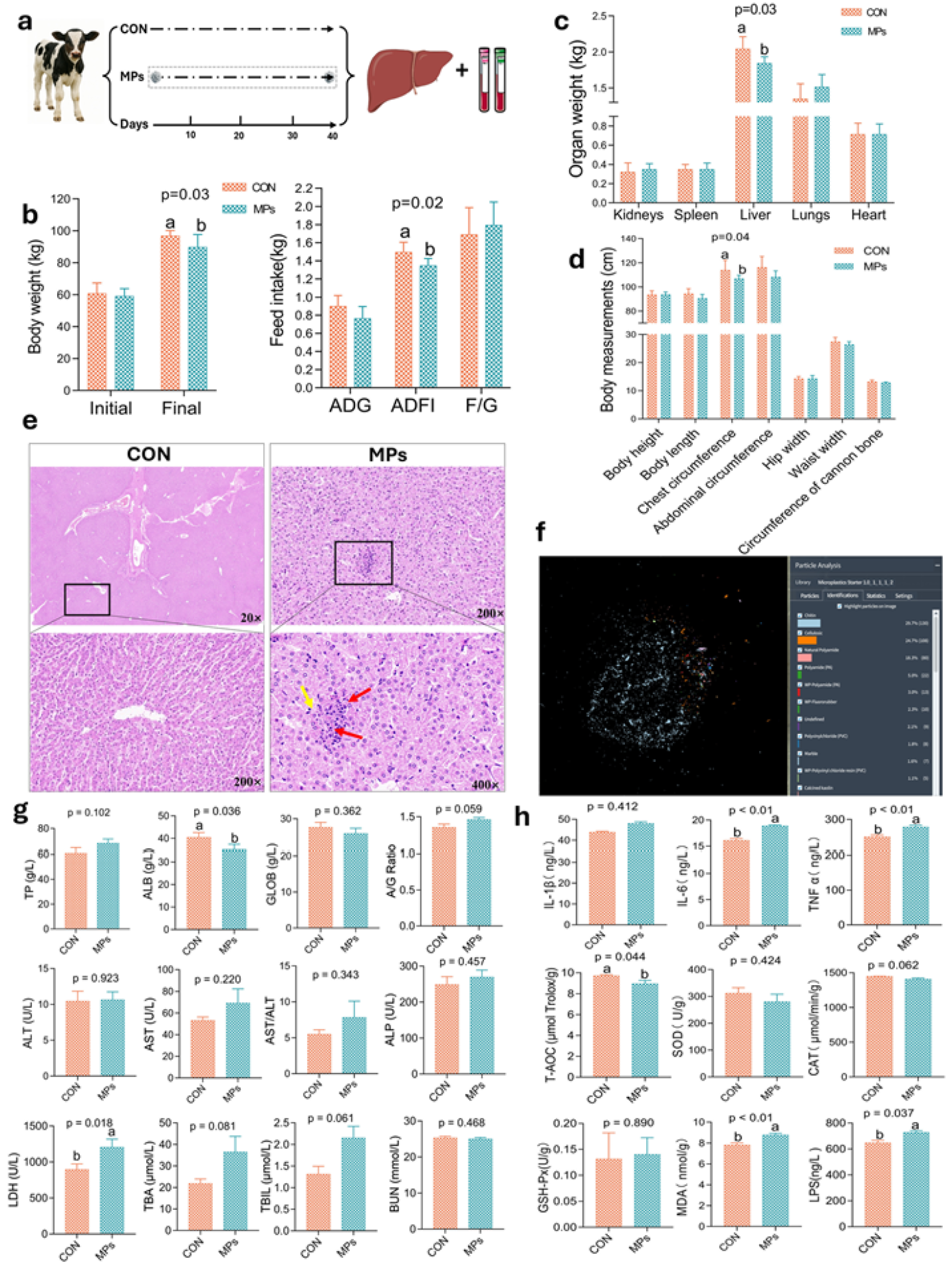
图2 | MPs诱导的肝毒性
- (a) 试验设计流程图:40 d暴露期,采集肝脏及血液样本
- (b) 终体重和采食量显著降低(p<0.05),平均日增重(ADG)和平均日采食量(ADFI)下降
- (c) 肝脏重量显著减轻(p=0.03)
- (d) 胸围显著减小(p=0.04)
- (e) H&E染色显示MPs组肝细胞核碎裂/溶解、点状淋巴细胞浸润(红箭头)及点状坏死(黄箭头)
- (f) 肝脏组织LDIR检测:未检出PE-MPs(n=3)
- (g) 血清生化指标:LDH显著升高(p=0.01),ALB显著降低(p=0.036)
- (h) 肝脏炎症因子:IL-6、TNF-α显著上调(p<0.05),LPS水平显著升高(p=0.037)
核心结论:MPs暴露损害犊牛增重和肝脏发育,但未在肝组织中直接检出PE微塑料,提示肝损伤可能由LPS介导的炎症反应引起,而非微塑料直接蓄积。
肠道屏障完整性受损
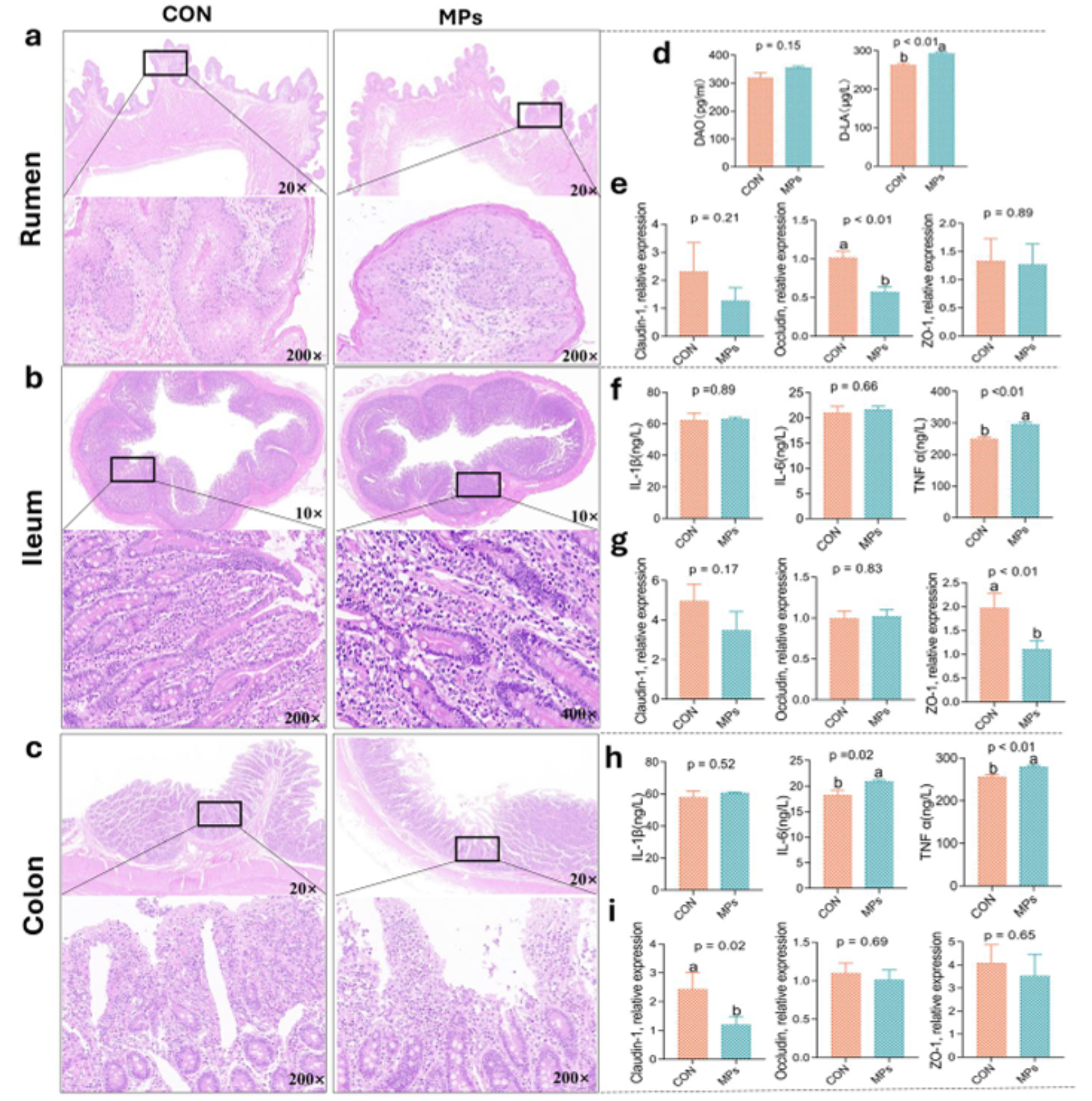
图3 | MPs破坏肠道屏障完整性
- (a-c) 瘤胃、回肠和结肠H&E染色:MPs组回肠和结肠出现明显炎症细胞浸润和充血,瘤胃损伤相对较轻
- (d) 血清D-LA水平显著升高(p<0.01),DAO有升高趋势,提示肠道通透性增加
- (e) 瘤胃Occludin mRNA表达下调
- (g) 回肠ZO-1 mRNA表达显著下调(p<0.01)
- (i) 结肠Claudin-1 mRNA表达显著下调(p<0.05)
- (f,h) 回肠和结肠IL-6、TNF-α水平显著升高(p<0.05)
机制提示:MPs暴露通过下调紧密连接蛋白(Occludin、ZO-1、Claudin-1)破坏肠道屏障,增加LPS易位风险。
肌肉组织脂质代谢紊乱
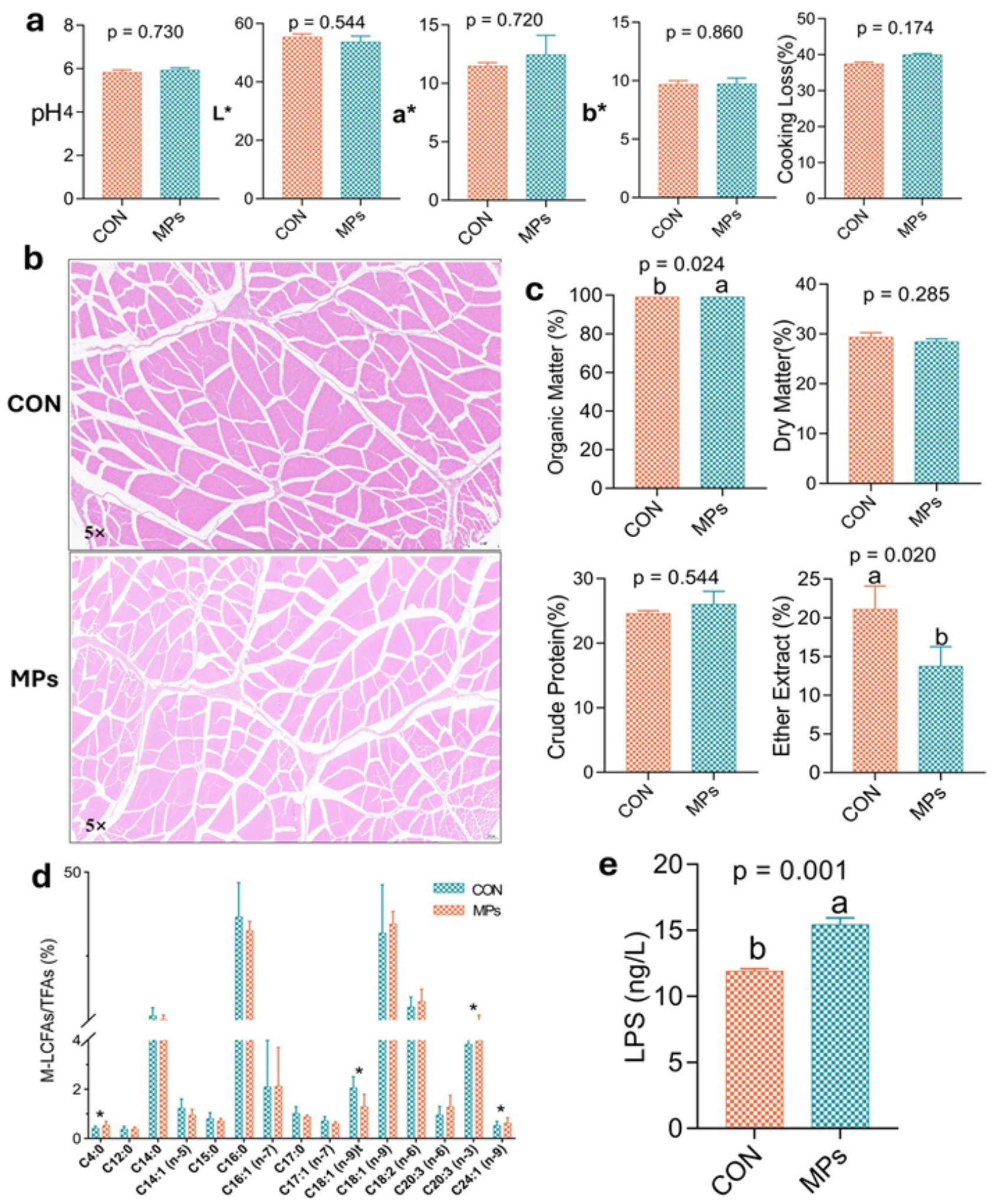
图4 | MPs影响肌肉脂肪与LPS浓度
- (a) 肉品质参数(pH₂₄ₕ、肉色Lab*、蒸煮损失)无显著差异
- (b) H&E染色显示肌肉组织结构无显著异常
- (c) 粗脂肪含量(Ether Extract)显著降低(p=0.020)
- (d) 多种中长链脂肪酸显著减少(*p<0.05)
- (e) 肌肉组织LPS水平显著升高(p=0.001)
重要发现:虽然MPs未造成肌肉组织结构性损伤,但显著扰乱脂质稳态,并促进促炎因子LPS在肌肉组织中沉积,对肉品安全构成潜在风险。
全身炎症与血液代谢改变
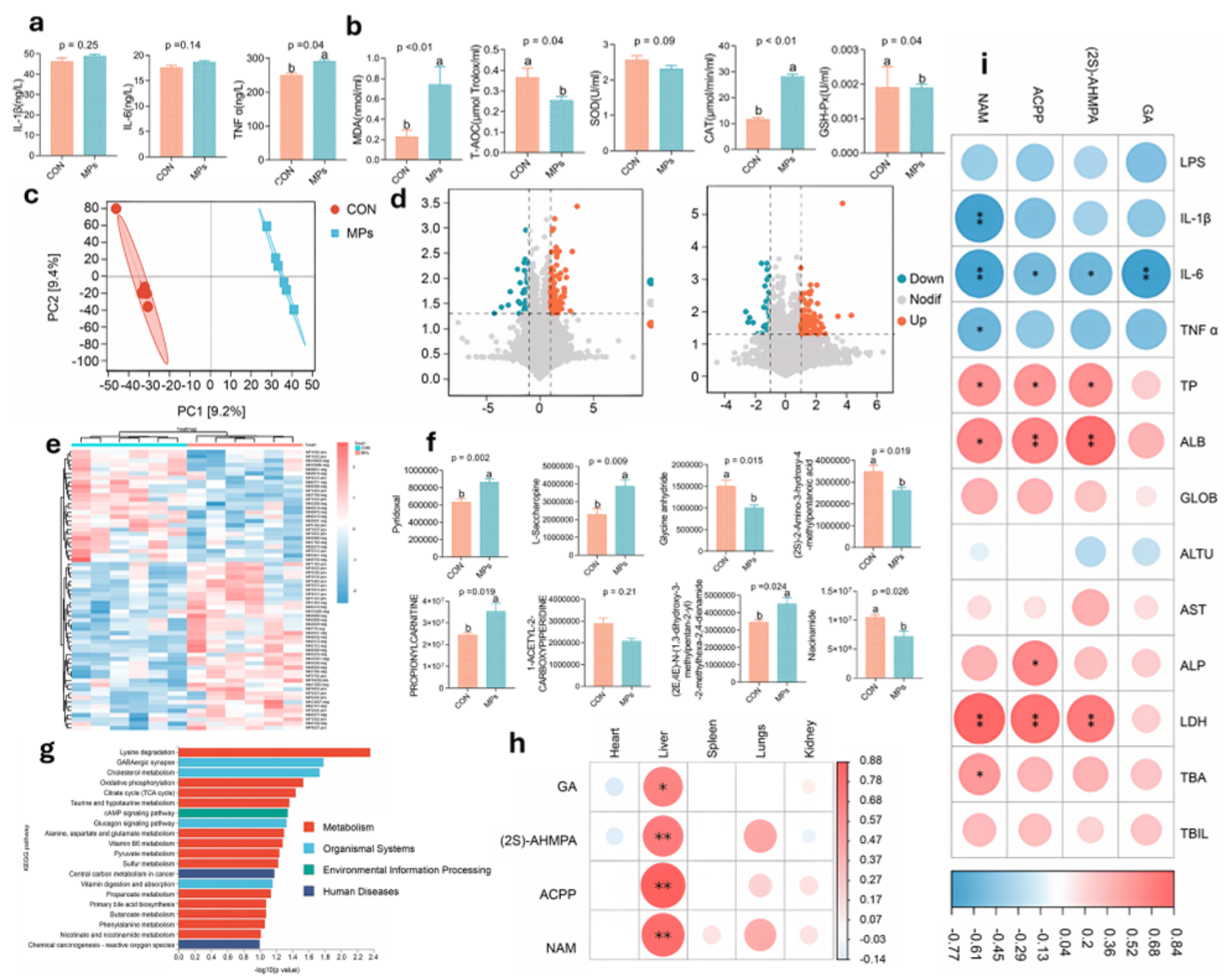
图5 | MPs诱导全身炎症及血液代谢变化
- (a) 血清TNF-α显著升高(p=0.04),IL-1β、IL-6有升高趋势
- (b) 氧化应激标志物:CAT和MDA显著升高(p<0.05),T-AOC和GSH-Px降低(p=0.04)
- (c) PCA得分图显示两组代谢谱明显分离
- (d) 火山图:65个差异代谢物(39个上调,26个下调)
- (e) 差异代谢物热图
- (f) 与肝脏重量正相关的4个关键代谢物:Pyridoxal、L-Saccharopine等
- (g) KEGG富集:赖氨酸降解和胆固醇代谢通路显著富集
- (h,i) 相关性热图:烟酰胺(NAM)与IL-1β、TNF-α负相关(p<0.05)
代谢组学洞察:MPs通过LPS易位引发全身炎症,血液代谢改变可能由赖氨酸降解和胆固醇代谢通路介导。
瘤胃微生物群落重塑
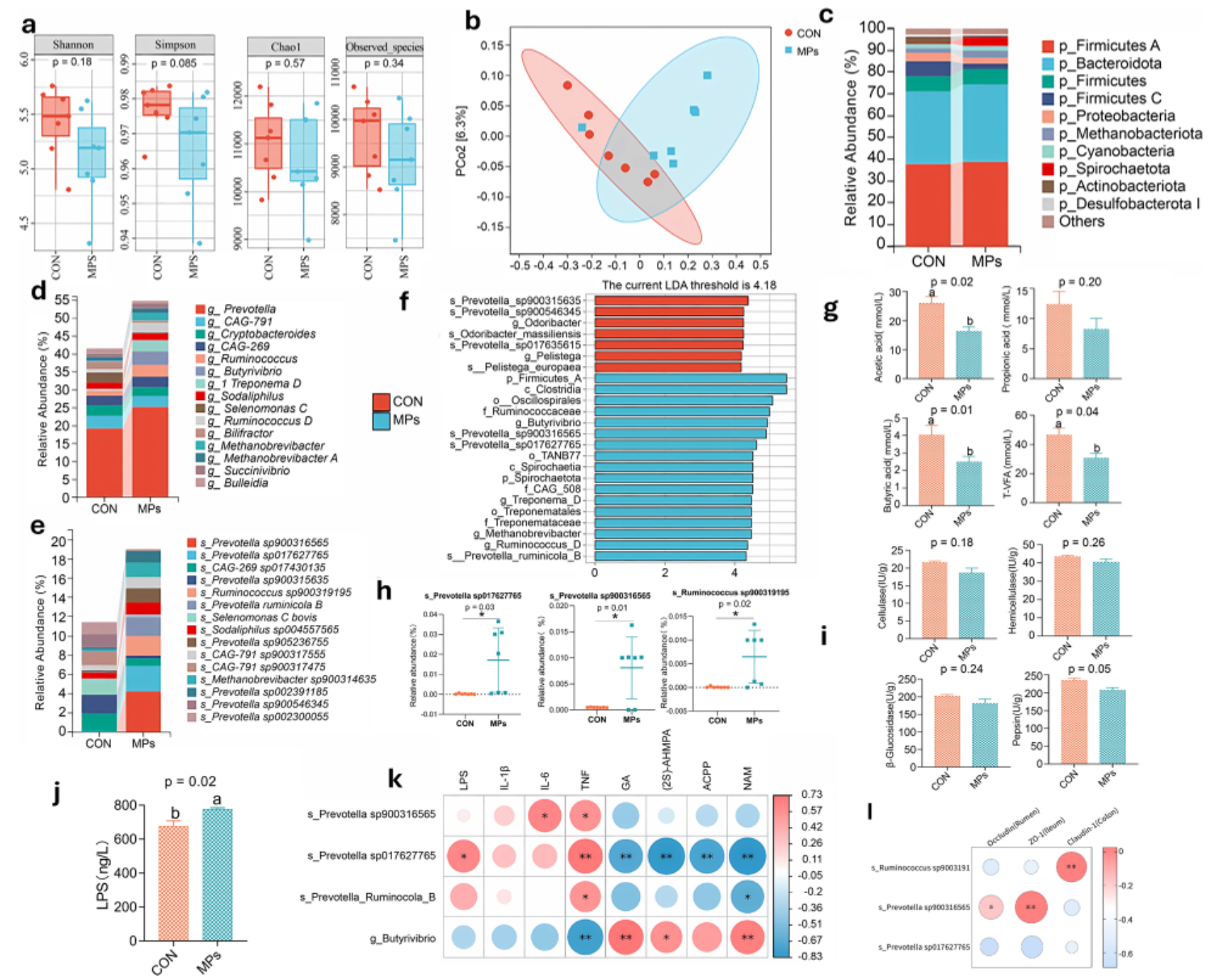
图6 | MPs改变瘤胃微生物群落
- (a) α多样性指数(Chao1、Shannon等)无显著差异
- (b) PCoA分析显示两组微生物群落结构显著分离
- (c) 门水平:厚壁菌门、拟杆菌门、变形菌门为优势菌群
- (d,e) 属/种水平:Prevotella属相对丰度增加
- (f) LEfSe分析:MPs组富集17个差异物种(vs CON组7个),包括s_Prevotella sp017627765、p_Spirochaeta等
- (g) 乙酸浓度显著降低(p=0.02),丙酸、丁酸无显著变化
- (h) 三个Prevotella物种在MPs组显著富集(p<0.05)
- (j) 血液LPS浓度显著升高(p=0.02)
- (k,l) 相关性分析:Prevotella物种与LPS、炎症因子正相关,与紧密连接蛋白负相关
微生物机制:MPs选择性促进革兰氏阴性菌(Prevotella)增殖,这些菌群是LPS的主要生产者,为后续肝脏炎症提供内毒素来源。
微生物功能与LPS合成通路激
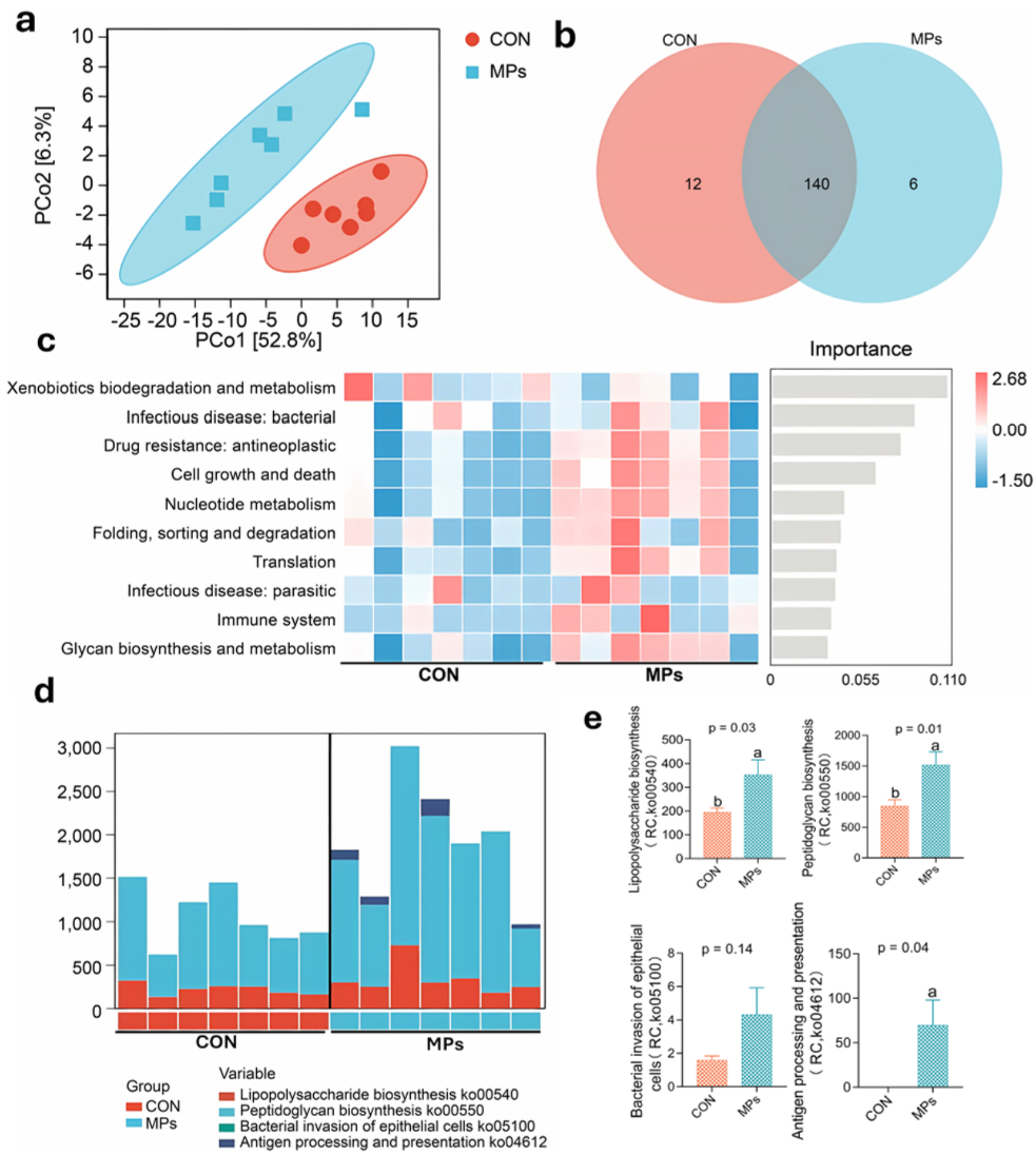
图7 | MPs激活LPS生物合成通路
- (a) 功能PCoA显示两组功能谱差异显著
- (b) Venn图:140个共享功能单元,CON组12个独特单元,MPs组6个
- (c) 随机森林分析:感染性疾病、免疫系统、聚糖生物合成等通路显著改变
- (d,e) 关键通路显著上调:
○ LPS生物合成(ko00540,p=0.03)
○ 肽聚糖生物合成(ko00550,p=0.01)
○ 细菌侵袭上皮细胞(ko05100,p=0.14)
○ 抗原加工与呈递(ko04612,p=0.04)
功能验证:宏基因组学证实MPs暴露显著激活瘤胃微生物的LPS合成通路,增加内毒素产生潜力。
瘤胃代谢物变化
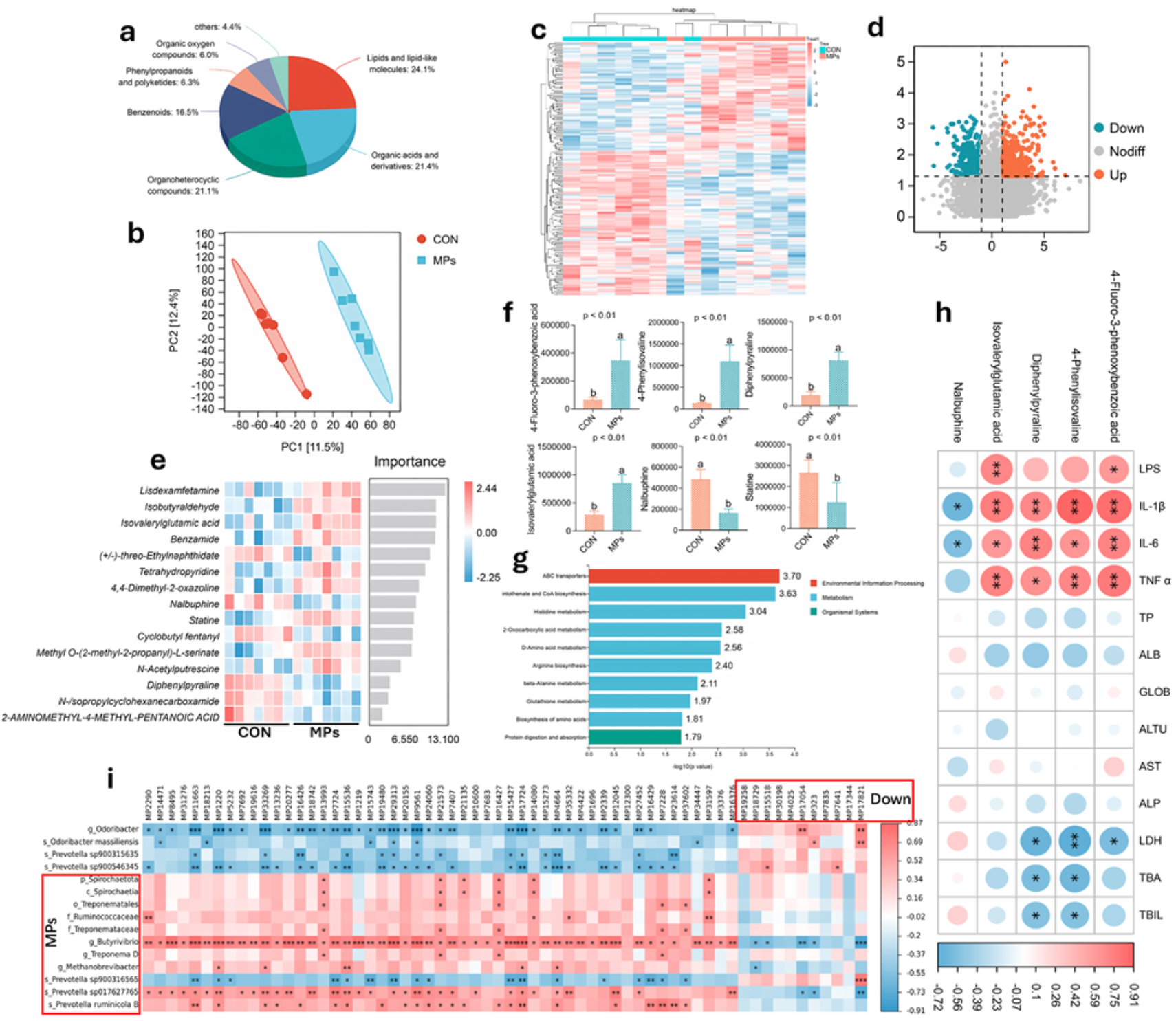
图8 | MPs改变瘤胃代谢谱
- (a) 代谢物分类:脂质及类脂分子(24.1%)、有机杂环化合物(21.1%)、有机酸及衍生物(21.4%)、苯类化合物(16.5%)
- (b) PCA显示两组代谢物明显分离
- (c) 代谢物表达模式热图
- (d) 火山图:173个差异代谢物(74个上调,99个下调)
- (e) 随机森林重要代谢物:Lisdexamfetamine、Isobutyraldehyde、Isovalerylglutamic acid等在MPs组上调
- (f) 关键差异代谢物与肝功能相关指标
- (g) KEGG富集:ABC转运蛋白通路为主要富集通路
- (h) 相关性热图:4-Fluoro-3-phenoxybenzoic acid和Isovalerylglutamic acid与LPS、IL-1β、IL-6、TNF-α显著正相关(p<0.05)
- (i) 差异微生物与差异代谢物相关性:MPs组微生物与上调代谢物多呈正相关
代谢-微生物互作:Isovalerylglutamic acid与LPS显著正相关,可能是连接瘤胃微生物失调与肝脏炎症的关键代谢标志物。
肝脏转录组与炎症信号通路
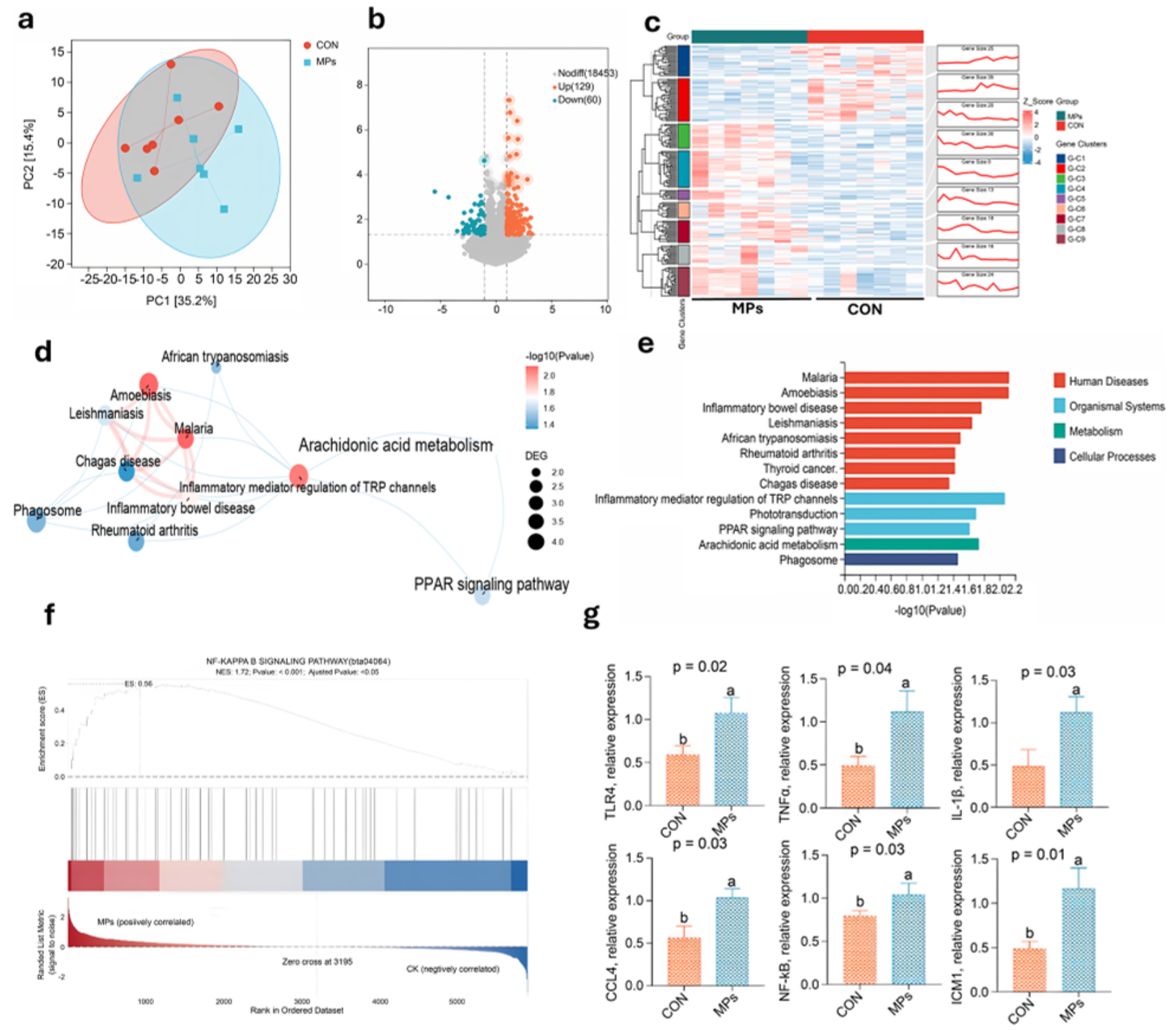
图9 | 肝脏转录组揭示TLR4/NF-κB通路激活
- (a) PCA显示肝脏转录组明显分离
- (b) 火山图:189个差异表达基因(129个上调,60个下调)
- (c) DEGs表达模式热图及聚类分析
- (d,e) KEGG富集:TRP通道炎症介质调控、炎症性肠病、疟疾、阿米巴病等疾病通路显著富集
- (f) GSEA分析:NF-κB信号通路显著激活(NES=1.69,p<0.001)
- (g) qPCR验证:TLR4、TNF-α、IL-1β、CCL4、NF-κB、ICAM1 mRNA表达均显著上调(p<0.05)
分子机制:MPs暴露激活肝脏TLR4/MyD88/NF-κB信号级联,这是LPS诱导肝脏炎症的核心通路。
机制总结
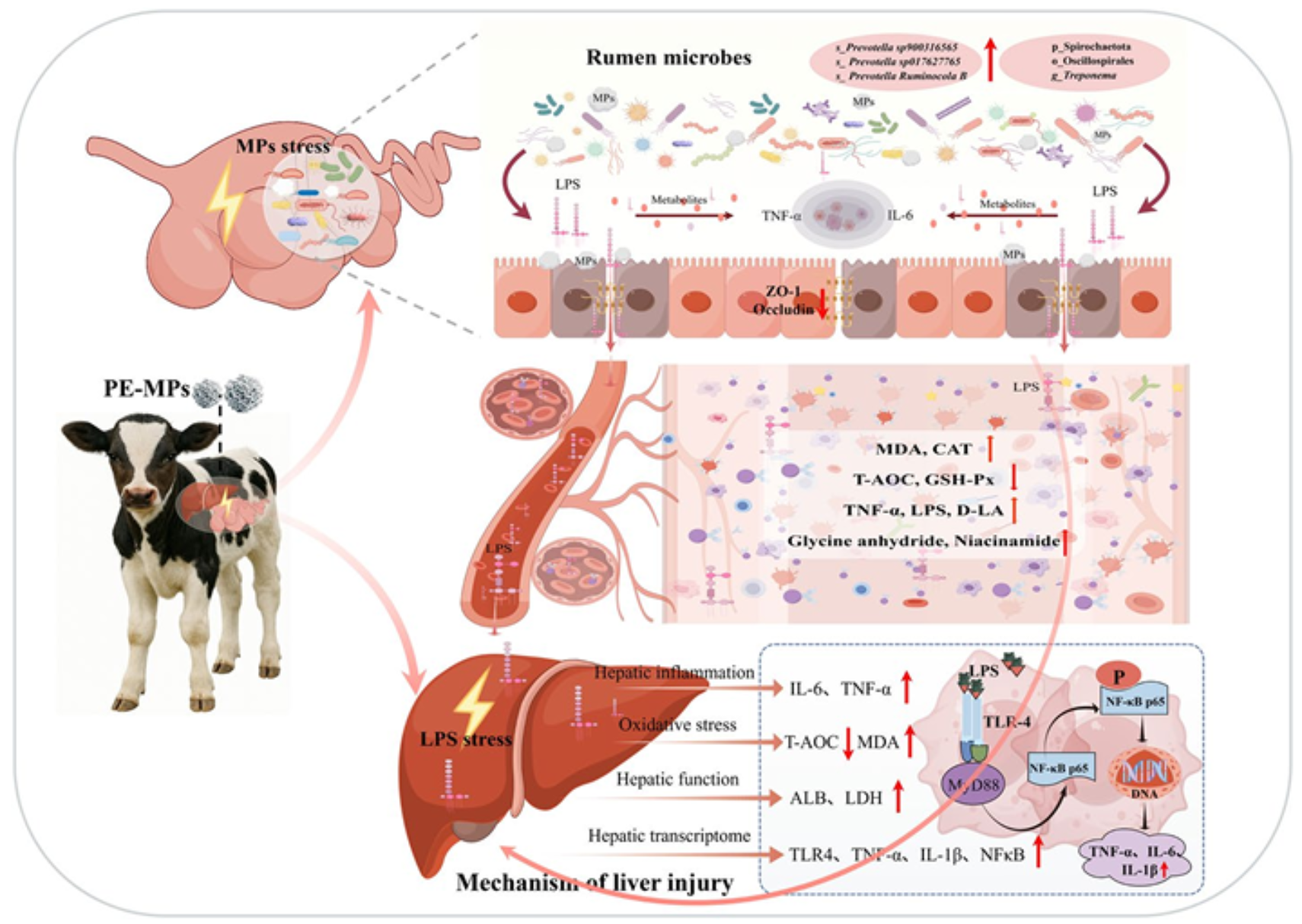
图10 | 机制模式图
MPs应激 → 瘤胃微生物群落重塑(Prevotella等革兰阴性菌富集)→ LPS生物合成通路激活 → 肠道屏障破坏(ZO-1、Occludin、Claudin-1下调)→ LPS易位入血 → 肝脏LPS应激 → TLR4/MyD88/NF-κB通路激活 → 肝脏炎症(IL-6、TNF-α↑)→ 肝功能损伤(ALB↓、LDH↑)
分子机制:MPs暴露激活肝脏TLR4/MyD88/NF-κB信号级联,这是LPS诱导肝脏炎症的核心通路。
研究结论
- 首次证实:MPs通过瘤胃微生物-肠道-肝脏轴间接诱导牛肝脏炎症,而非微塑料直接肝蓄积
- 关键介质:瘤胃来源的LPS是连接肠道微生物失调与肝脏损伤的核心因子
- 肉品安全:MPs导致肌肉组织LPS沉积和脂质代谢紊乱,对 livestock 产品安全构成潜在威胁
- 干预靶点:TLR4/NF-κB信号通路和ABC转运蛋白通路为缓解MPs毒性提供潜在靶标
原文链接
https://link.springer.com/article/10.1186/s40168-026-02399-5












